«Genwüste» steuert Embryonalentwicklung und Herzfunktion
Forschende der Universität Bern haben in Zusammenarbeit mit internationalen Partnern herausgefunden, dass ein als «Genwüste» bezeichneter Abschnitt des Erbguts eine wichtige Rolle in der Entwicklung des Embryos und des Herzens bei Mäusen und Menschen spielt. Die Studie liefert einen weiteren Beleg für die Bedeutung dieser genfreien DNA-Abschnitte für die Steuerung von Genen und bietet Ansätze, um Herzkrankheiten frühzeitig zu erkennen.
Das menschliche Erbgut (Genom) enthält spezifische DNA-Abschnitte, bekannt als «Gene», die als Bauplan für Proteine dienen. Wenn sich diese Abschnitte verändern und sogenannte Mutationen entstehen, kann dies zu Krankheiten oder zu Fehlbildungen des Embryos führen. Die Untersuchung des Genoms hat gezeigt, dass Mutationen auch in DNA-Bereichen ohne Bauplan für Proteine Probleme verursachen können. Diese «Genwüsten», die oft fälschlicherweise auch als «Junk-DNA» bezeichnet werden, spielen nämlich eine entscheidende Rolle bei der Steuerung der Gene und der Entwicklung.
In einer aktuellen, vom Schweizerischen Nationalfonds unterstützten Studie, hat ein internationales Forschungsteam unter der Leitung von Prof. Dr. Marco Osterwalder, Department for BioMedical Research (DBMR) der Universität Bern und Universitätsklinik für Kardiologie am Inselspital, Universitätsspital Bern, am Mausmodell untersucht, welche Rolle eine an das Shox2 Gen angrenzende Genwüste spielt. Das Shox2 Gen ist zentral für die Entwicklung der Gliedmassen und Herzfunktion, sowohl beim Menschen als auch bei Mäusen. In Zusammenarbeit mit Prof. John Cobb von der Universität Calgary in Kanada, mit dem Lawrence Berkeley National Laboratory, USA, und weiteren Partnern konnte das Forschungsteam zeigen, dass die an Shox2 angrenzende Region wichtige Elemente enthält, die dessen Aktivität steuern. Die Studienergebnisse wurden kürzlich in Nature Communications publiziert.
Genwüsten enthalten wichtige Steuerungselemente
Frühere Untersuchungen in Mäusen hatten gezeigt, dass es zu schweren Herzproblemen (Arrhythmien) und sogar zum Tod des Embryos kommen kann, wenn Shox2 nicht richtig funktioniert. Mutationen in der menschlichen Variante dieses Gens wurden ebenfalls mit Arrhythmien in Verbindung gebracht. Es war auch bekannt, dass die Genwüste rund um Shox2, bei Menschen und Mäusen sehr ähnlich ist. Wie die Aktivität des Gens im Embryo aber genau gesteuert wird, war bisher unklar. Frühere Studien haben zudem auch gezeigt, dass nicht alle Genwüsten, trotz ihrer teilweise immensen Ausdehnung, wichtig für die Embryonalentwicklung sind.
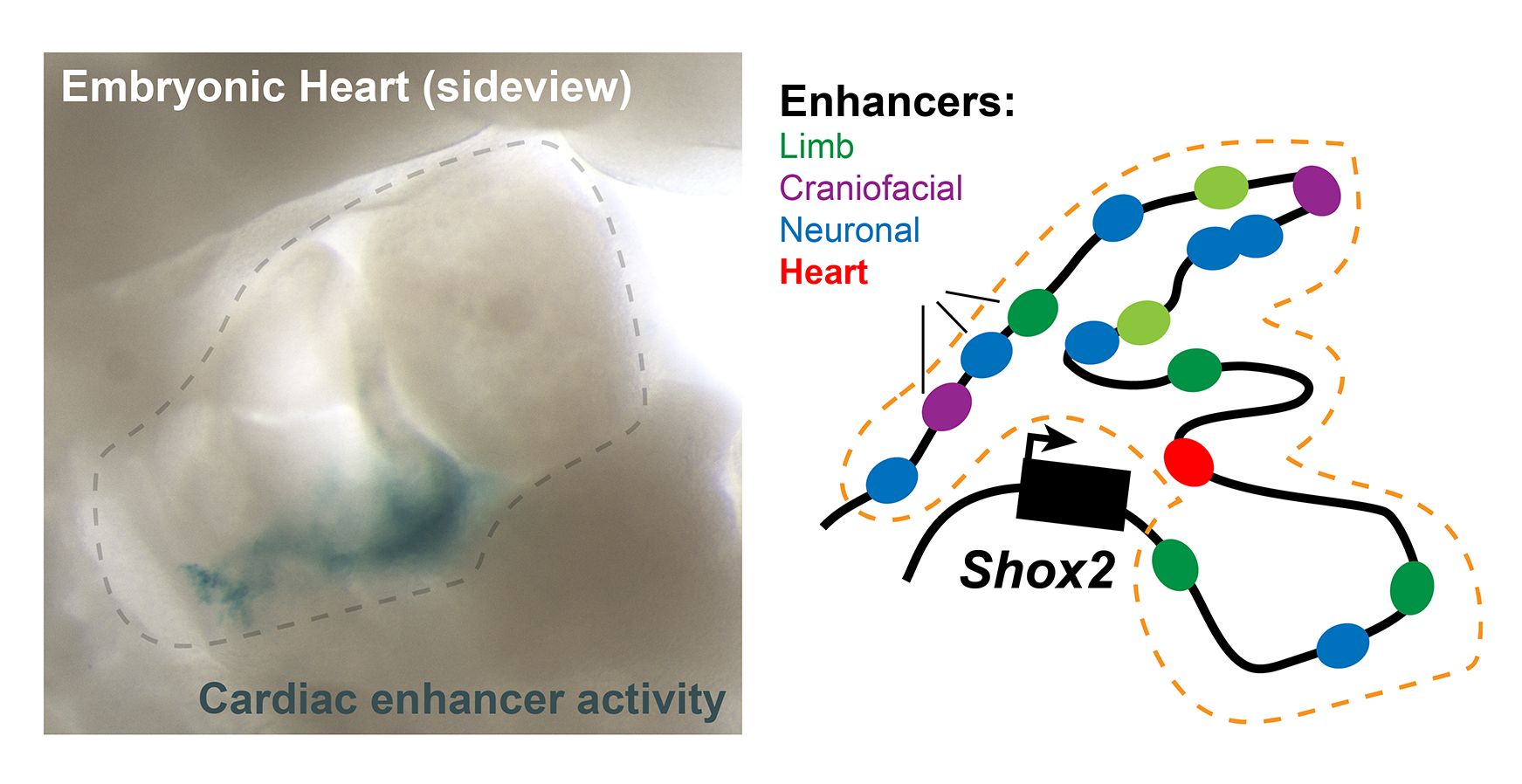
Die aktuelle Studie zeigt nun aber, dass der vermeintlich weitgehend "leere" DNA-Abschnitt neben dem entwicklungsbiologisch wichtigen Shox2-Gen insgesamt 15 Steuerelemente, so genannte Enhancer, enthält. Diese Enhancer steuern, wie, wann und wo das Gen während der Embryonalentwicklung aktiv ist.
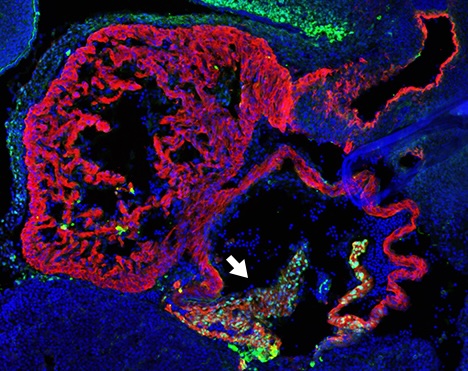
Ein Beispiel für die Bedeutung dieser Enhancer ist ihre Rolle in der Herzentwicklung. «In unserer Studie konnten wir zeigen, dass ein bestimmter Enhancer in der Genwüste die Aktivität des Shox2 Gens in den Zellen des sich entwickelnden Herzens bei Mäusen mitreguliert. Dies ist besonders wichtig, weil Shox2 eine Schlüsselrolle bei der Bildung des Sinusknotens spielt. Dieser gilt als natürlicher Herzschrittmacher, indem er elektrische Impulse erzeugt, die den Herzschlag kontrollieren», erklärt Marco Osterwalder, Co-Letztautor der Studie.
Potenzial für die genetische Diagnostik
Bisher gab es nur wenige Beispiele für solche genfreien Abschnitte, die für das Überleben von Mäuseembryonen und deshalb mit grosser Wahrscheinlichkeit auch für menschliche Embryonen zentral sind. «Die vorliegende Studie identifiziert nicht nur eine wichtige Genwüste im Erbgut, sondern zeigt auch wie komplex die Mechanismen sind, die der Steuerung von Entwicklungsgenen zugrunde liegen. Die neuen Ergebnisse können uns dabei helfen besser zu verstehen, wie Enhancer funktionieren und wie einzelne Gene in verschiedenen Zelltypen und Geweben des Embryos zeitgleich aktiv sind», sagt Osterwalder. Die Forschungsgebiete der funktionellen Genomik und der Erforschung von Krankheiten, die durch defekte Enhancer entstehen sind noch relativ neu und stehen im Zentrum moderner Forschungsansätze der Präzisionsmedizin. An der Medizinischen Fakultät der Universität Bern werden diese Schwerpunkte derzeit auch im Rahmen von «PACE», dem «Lighthouse» Projekt des Berner Zentrums für Präzisionsmedizin (BCPM) verfolgt.
Laut den Forschenden sind die Resultate besonders relevant für die «Kartierung» des menschlichen Genoms und könnten insbesondere in der modernen personalisierten Medizin für die genetische Diagnostik von grosser Bedeutung sein. Beispielsweise könnten genetische Tests, die Mutationen in solchen Genwüsten finden, dazu beitragen, das Risiko für bestimmte Geburtsfehler oder Herzkrankheiten wie beispielsweise Arrhythmien frühzeitig zu erkennen und entsprechend zu behandeln.
«Als Teil des Cardiovascular Disease Programms am DBMR und des Cardiovascular Research Clusters (CVRC) der Universität Bern und des Inselspitals werden wir die Erkenntnisse aus unserer Studie nutzen, um herauszufinden, wie die Entwicklung des Sinusknoten im Genom verankert ist», sagt Osterwalder. Ziel der Forschenden ist es, alle Steuerelemente mit Aktivität im Herzen innerhalb der untersuchten Genwüste zu identifizieren und zu untersuchen, ob diese von krankheitsrelevanten Mutationen betroffen sein könnten. «Diese Erkenntnisse könnten wichtige Beiträge zur genetischen Diagnostik und zur Behandlung von Herzrhythmusstörungen leisten», sagt Osterwalder abschliessend.
Angaben zur Publikation:Abassah-Oppong, S., Zoia, M., Mannion, B.J. et al. A gene desert required for regulatory control of pleiotropic Shox2 expression and embryonic survival. Nat Commun 15, 8793 (2024). https://doi.org/10.1038/s41467-024-53009-7 |
Department for BioMedical Research (DBMR)Das Department for BioMedical Research (DBMR) der Medizinischen Fakultät der Universität Bern wurde 1994 von der Universität Bern und dem Inselspital, Universitätsspital Bern gegründet. Das DBMR ist in 13 Forschungsprogramme mit rund 100 teilnehmenden Einzellabors und mehreren unabhängigen Forschungslabors unterteilt, deren Forschung sich über alle biomedizinischen Bereiche erstreckt. Um die Lücke zwischen Labor und Krankenbett zu schliessen, fördert das DBMR klinische Forschung mit einem starken Schwerpunkt auf der Entwicklung translationaler Ansätze, dem Einsatz von «Omics» und anderen Spitzentechnologien sowie einer umfassenden Zusammenarbeit zwischen laborgestützter und patientenorientierter klinischer Forschung. Das DBMR setzt sich auch für die Förderung des wissenschaftlichen Nachwuchses ein. |
Cardiovascular Research ClusterDer Cardiovascular Research Cluster (CVRC) Bern wurde 2015 als lokales Netzwerk gegründet, um die Sichtbarkeit und das Bewusstsein für die laufende kardiovaskuläre Forschung in Bern zu erhöhen, die Zusammenarbeit zwischen Forschenden und Klinikern und Klinikerinnen der Universität Bern und des Inselspitals zu fördern, das Ausbildungsumfeld für Nachwuchsforschende zu bereichern und einen Rahmen und logistische Unterstützung für teamübergreifende und/oder interdisziplinäre Projekte zu bieten. Ziel ist es, Berns Position als führendes Zentrum für kardiovaskuläre Forschung auf nationaler und internationaler Ebene zu stärken und seine Wettbewerbsposition für die Zukunft zu sichern, indem es Grundlagen-, translationale und klinische Partnerschaften fördert, das Ausbildungsprogramm für Doktorierende bereichert und die Sichtbarkeit und Attraktivität Berns für Forschende im Bereich Herz-Kreislauf-Erkrankungen erhöht. Es hat eine starke Gemeinschaft aufgebaut und die Verbindungen zwischen den Berner Herz-Kreislauf-Forschern gestärkt. Das CVRC umfasst mittlerweile über 400 Mitglieder aus 15 lokalen Instituten und Abteilungen. |
PACE - Dem plötzlichen Herzstillstand auf der SpurDas interdisziplinäre Projekt PACE (Precision Diagnosis and Therapy in CArdiac ChannelopathiEs) wurde 2023 als «Lighthouse Project» des Bern Center for Precision Medicine (BCPM) ausgewählt und hat einen präzisen, personalisierten Therapieansatz bei Herzrhythmusstörungen zum Ziel. Das Projekt wird geleitet von Prof. Dr. Katja Odening, Ordinaria für Translationale Kardiologie, zusammen mit den weiteren Projektpartnern und Partnerinnen, Prof. Nadia Mercader, Ordinaria für Anatomie, Prof. Christiane Zweier, Ordinaria für Humangenetik, Prof. Jean-Louis Reymond, Ordinarius für Chemie und Prof. Marco Osterwalder, und seit Anfang 2024 an der Universität Bern durchgeführt. Bei jungen Personen steht häufig eine erblich bedingte Ionenkanalerkrankung mit dem plötzlichen Herzstillstand im Zusammenhang. Deshalb konzentrieren sich die Forschenden in einem ersten Schritt darauf, die krankheitsverursachenden Genvarianten im Erbgut der Patientinnen und Patienten zu identifizieren. Darüber hinaus wird auch die Rolle von Genvarianten mit unklarer Bedeutung und von genetischen Modifikatoren wie Enhancern untersucht. Um die Bedeutung dieser Genvarianten und Modifikatoren besser zu verstehen, werden Experimente in Zellkultur und je nach Fokus spezifisch mit Modellorganismen (Fruchtfliege, Zebrafisch, Maus oder Kaninchen) kombiniert. Dieser Ansatz soll schliesslich Rückschlüsse auf Krankheitsmechanismen beim Menschen sowie neue Therapieansätze ermöglichen. Mehr Informationen |
06.11.2024