Herzinfarkt bis in die kleinsten Gefässe bekämpfen
Berner Forschende haben eine neue Methode gegen die Verstopfung winziger Herzkranzgefässe nach einem Herzinfarkt mitentwickelt und getestet. Der neue Ansatz, der im Zusammenspiel von Grundlagenforschung, Klinik und Industrie entwickelt wurde, bietet eine Behandlungsmöglichkeit gegen das Absterben von Herzgewebe nach einem Infarkt, das für eine schlechte Langzeitgesundheit der Betroffenen verantwortlich ist.
Bei einem Herzinfarkt wird die Versorgung des Herzmuskels mit Sauerstoff und Nährstoffen durch ein Blutgerinnsel in einer der grossen Koronararterien blockiert. Selbst nach einer sogenannten Rekanalisierung dieser Arterie mittels eines Stents kommt es bei 40-60 % aller Patientinnen und Patienten zu sekundären Blockaden in der Durchblutung der kleinsten Herzgefässe (Microvascular Obstruction, MVO). Dabei kann Herzgewebe absterben, was bei Patientinnen und Patienten langfristig zu einer schlechteren Gesundheit führt. Davon sind in der Schweiz rund 200’000 Personen jährlich betroffen.
«MVO ist eine unterdiagnostizierte Erkrankung, da sie bei der Akutbehandlung nicht leicht zu erkennen ist und es bisher keine Behandlung dafür gibt», sagt Dominik Obrist vom ARTORG Center for Biomedical Engineering der Universität Bern. Bisher werden bei Herzinfarkten nur die grösseren verstopften Arterien mittels Kathetern behandelt – auch, weil die Katheter wegen ihrer Grösse nicht in kleinere Gefässe vordringen können. Ein Katheter ist ein dünner Schlauch, der in den Körper eingeführt wird, um die Blutgefässe zu untersuchen und zu behandeln.
«Die Beseitigung von Verstopfungen in grösseren Gefässen verhindert nicht, dass Herzgewebe weiter unten im Gefässbaum abstirbt, weil es nicht mehr vom Blutfluss erreicht wird», sagt Obrist. Seine Gruppe für Cardiovascular Engineering am ARTORG Center der Universität Bern konnte in einer langjährigen Zusammenarbeit mit klinischen Partnern sowie einem Medizintechnik-startup erstmals eine neue Technik entwickeln, die eine Diagnose und Behandlung von MVO ermöglicht. Die Methode wird nun klinisch getestet und weiter verfeinert.
Forschen in Mikrometergrösse
Um in die Gefässe vordringen zu können, die etwa so fein sind wie ein menschliches Haar (Durchmesser 50 Mikrometer), untersuchten die Forschenden zunächst den Blutfluss im Herzen anhand eines neuartigen Modells der Koronargefässe. In einer ersten Studie testeten sie einen neu entwickelten Ballonkatheter, mit dem MVO durch Aufblasen des Ballons an der Stelle der verstopften Arterie korrekt diagnostiziert werden kann. Dabei werden der Druck und der Widerstand des Blutflusses gemessen, um so MVO von Druckverhältnissen unter gesunden anatomischen Verhältnissen unterschieden zu können.
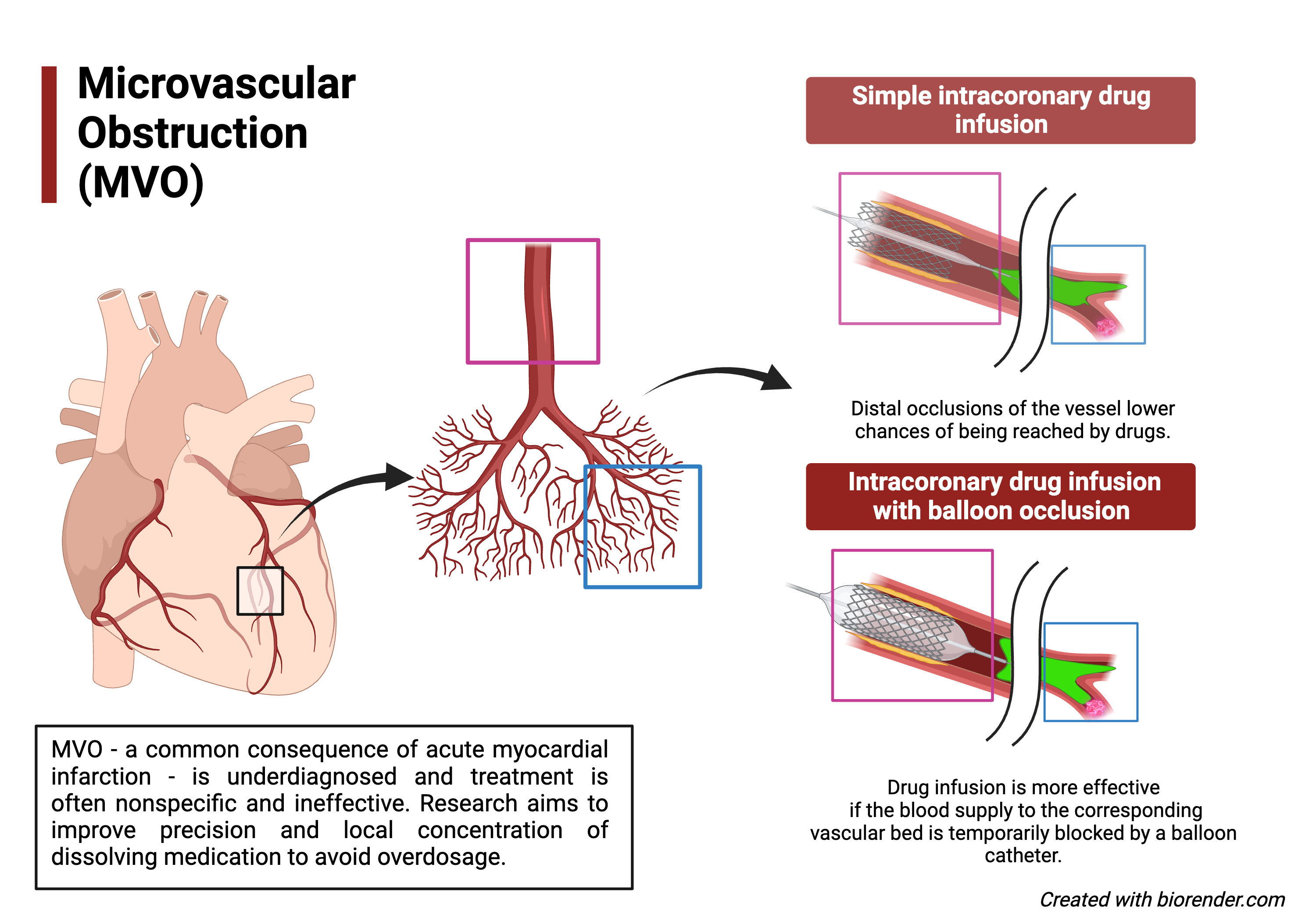
In einem zweiten Schritt wurde untersucht, wie gerinnselauflösende Medikamente in diese winzigen Verzweigungen eingeflösst werden können. «Wenn eine Arterie verstopft ist, sucht sich das Blut einen anderen Weg und umgeht den verstopften Zweig. Dieses Phänomen macht es aber sehr schwierig, Medikamente in den verstopften Ast einzuführen, da sie direkt in die gesunden Gefässe daneben ausgewaschen werden», erklärt Yannick Rösch vom ARTORG Center. «Wir konnten zeigen, dass das Aufblasen des Ballonkatheters, der zugleich Medikamente einflösst, genügend hohe Konzentrationen dieser Medikamente an die blockierten Gefässe liefert. Auf diese Weise können wir die Verstopfung erreichen, und die Medikamentendosierung könnte sogar reduziert werden, da wir keinen Auswascheffekt haben.»
Enge Zusammenarbeit von Wissenschaft, Klinik und Industrie
«Unser Projekt ist ein Paradebeispiel für die vernetzte interdisziplinäre Zusammenarbeit auf dem Medizinalstandort Bern – zwischen Forschenden der Universität Bern, klinischen Expertinnen des Inselspitals und der lokalen Industrie, zusammen mit der Expertise von weiteren Schweizer Partnern, um möglichst rasch Lösungen zu den Patientinnen und Patienten zu bringen», sagt Obrist. Diese vernetzte Forschung zu MVO führte zur Gründung des start-ups CorFlow Therapeutics AG. Dessen Technologie ermöglicht es, noch während der Erstbehandlung von Herzinfarkt-Patientinnen und -patienten im Katheter-Labor eine MVO-Diagnose zu stellen und gleich nach dem Setzen von Stents mit der MVO-Behandlung zu beginnen. Zu den akademischen Partnern gehören die ETH Zürich, die Universität Zürich, die Hochschule für Technik OST in Buchs (SG) und die Universitätsklinik für Kardiologie des Inselspitals Bern.
Neben In-vivo-Tests des neuen Medizinprodukts und einer ersten klinischen Studie am Menschen haben die Forschenden ihr Versuchsmodell mit biologischem Fachwissen verfeinert und kürzlich die Wirksamkeit von gerinnselauflösenden Medikamenten an Mikroblutgerinnseln in einem mikrofluidischen Chip untersucht, der die Strömungsmechanik innerhalb kleinster Blutgefässe simuliert. «Die Medikamente zur Auflösung von Blutgerinnseln weisen in hoher Dosierung schwere Nebenwirkungen auf. Wir konnten nun aber zeigen, dass schon geringste Mengen dieser bekannten und klinisch verwendeten Medikamente in der Lage sind, einzelne Mikroblutgerinnsel aufzulösen», sagt Anastasia Milusev, wissenschaftliche Mitarbeiterin am ARTORG Center. «Damit wird es erstmals möglich, gezielt und niedrig dosiert Blutgerinnsel aufzulösen. Jetzt müssen wir alle Teile des Puzzles zusammenfügen, um die Therapie für MVO für Patientinnen und Patienten verfügbar zu machen.»
Publikationen:Rösch Y., Stolte T., Weisskopf M., Frey S., Schwartz R., Cesarovic N., Obrist D. Efficacy of catheter-based drug delivery in a hybrid in-vitro model of cardiac MVO with porcine microthrombi, Bioeng Transl Med.2023; e10631. https://doi.org/10.1002/btm2.10631 Rösch Y., Eggenberger D., Kuster Y., Widmer L., Frey S., Schwartz R., Nef C., Ulmer J., Obrist D. Enhanced Drug Delivery for Cardiac Microvascular Obstruction with an Occlusion-Infusion-Catheter, Ann Biomed Eng, 2023. https://doi.org/10.1007/s10439-023-03142-z Thirugnanasambandam M., Frey S., Rösch Y., Mantegazza A., Clavica F., Schwartz R., Cesarovic N., Obrist D. Effect of Collateral Flow on Catheter-Based Assessment of Cardiac Microvascular Obstruction, Ann Biom Eng, 2022. https://doi.org/10.1007/s10439-022-02985-2 |
Forschungsgruppe Cardiovascular Engineering am ARTORG CenterDie ARTORG-Forschungsgruppe Cardiovascular Engineering untersucht kardiovaskuläre Strömungen und Krankheiten wie Herzklappenerkrankungen und Herzinfarkt. Ihre Forschung zielt darauf ab, die langfristige Haltbarkeit und Biokompatibilität von Implantaten zu verbessern und neue diagnostische und therapeutische Instrumente für die klinische Praxis zu entwickeln. Die translationalen Forschungsprojekte befassen sich mit unmittelbaren klinischen Bedürfnissen, die gemeinsam mit den klinischen Partnern in der Kardiologie und der kardiovaskulären Chirurgie des Inselspitals ermittelt wurden, die eng in die Projektteams eingebunden sind. Das Team betreibt ein experimentelles Strömungslabor mit moderner Messtechnik und ein Computerlabor zur Modellierung von Strömungen im Herz und in Blutgefässen. Zu den experimentellen Einrichtungen gehören Hochgeschwindigkeitskameras und laserbasierte Methoden zur dreidimensionalen Quantifizierung von Strömungen. Die Gruppe entwickelt und nutzt massgeschneiderte Computermodelle und Supercomputer, um biomedizinische Strömungssysteme zu untersuchen. |
19.03.2024