Neue Gene entdeckt, die den Erfolg einer Krebstherapie beeinflussen
Eines der grossen Rätsel der Krebsforschung ist, wieso bestimmte Patientinnen und Patienten auf eine Strahlentherapie besser ansprechen als andere. Forschende der Universität Bern haben nun entdeckt, welche Gene hierfür eine wichtige Rolle spielen. Daraus ergeben sich neue Erkenntnisse für die Krebsbehandlung.
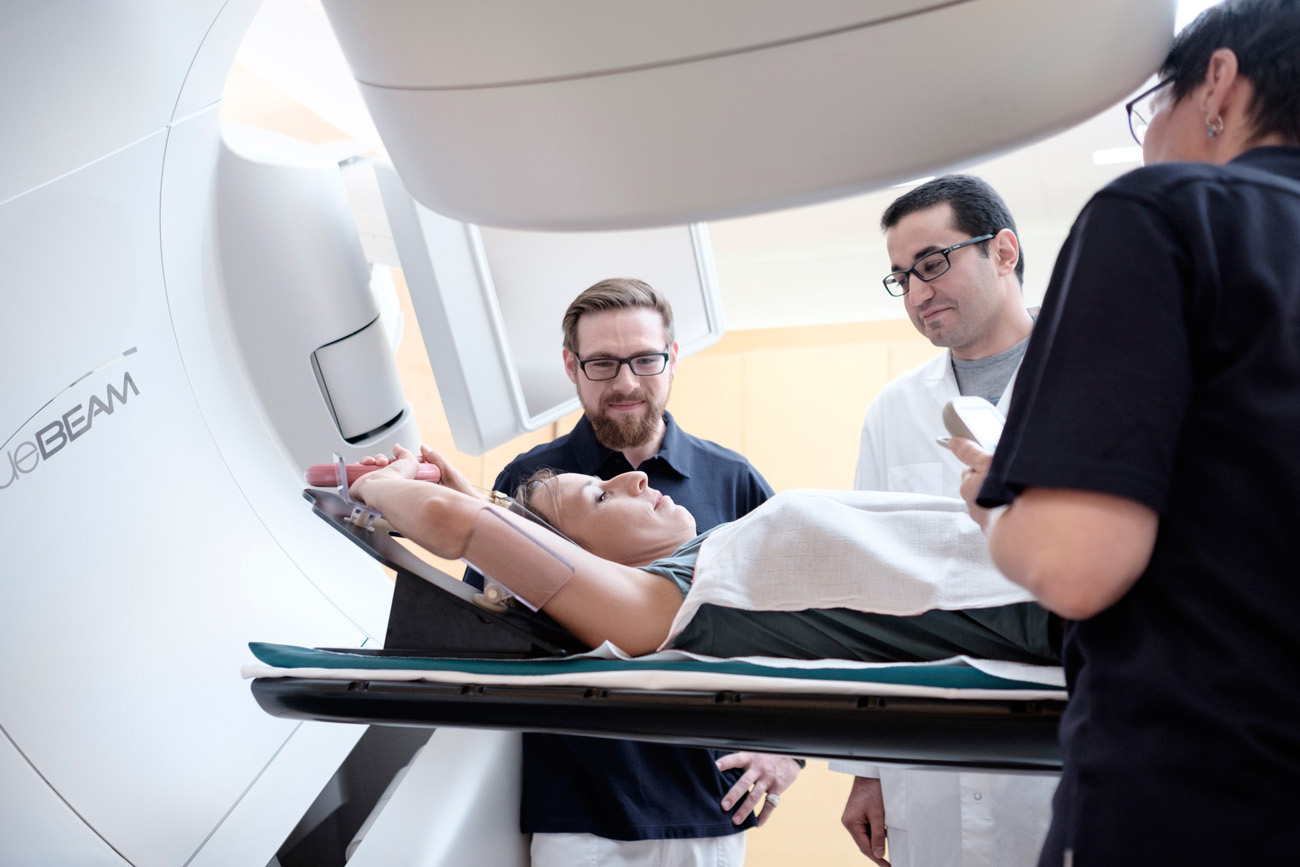
Die Strahlentherapie ist ein Grundstein der heutigen Krebstherapie. Rund die Hälfte aller krebserkrankten Menschen wird mit einer sogenannten Radiotherapie behandelt. Hierzu werden die Patientinnen und Patienten in der Regel über mehrere Wochen täglich bestrahlt. Obwohl diese Therapie bei vielen Menschen zur Heilung beiträgt, haben andere kaum einen Nutzen davon. Die genauen Ursachen dieser Unterschiede sind unklar. Mit Hilfe von genetischen Testverfahren hat nun ein Team um Prof. Sven Rottenberg von der Universität Bern in enger Zusammenarbeit mit dem niederländischen Krebsforschungszentrum in Amsterdam Gene identifiziert, die hierfür eine wichtige Rolle spielen.
«Für viele Krebspatientinnen und -patienten, deren Angehörige und behandelnden Ärztinnen und Ärzten ist es enorm frustrierend, wenn nach einer mühsamen und wochenlangen Strahlentherapie der Erfolg ausbleibt», sagt Rottenberg. «Wir hoffen, dass unserer Erkenntnisse dazu beitragen die Aussichten auf Erfolg einer Strahlentherapie besser vorherzuzsagen.» Zudem können die Erkenntnisse dazu verwendet werden, neue Medikamente zu entwickeln, welche die Effizienz der Radiotherapie verbessern könnten. Die Resultate der Studie wurden nun im Journal «Cell Reports» publiziert.
Schlüssel-Gene für den Therapieerfolg
Das Ziel der Strahlentherapie ist die DNA der Krebszellen – also deren Bauplan – zu schädigen. Dieser enthält Mutationen, die das unkontrollierte Wachstum verursachen. Durch die Zerstörung der DNA der Krebszellen soll das Tumorwachstum gestoppt werden. Wie alle Zellen in unserem Körper verfügen die Krebszellen aber auch über Werkzeuge, um genau diese DNA-Schädigung wieder zu reparieren. Zwischen den Tumoren von einzelnen Krebskranken gibt es dabei grundlegende Unterschiede, welche Werkzeuge zur Verfügung stehen. Diese hängen mit den Genen zusammen, die jeweils die Information für diese Werkzeuge verschlüsseln. Die Forschenden um Rottenberg untersuchten mittels genetischen Screenings die Selbstreparatur von Krebszellen. Dabei stiessen sie auf entscheidende Schwachstellen: Wenn bestimmte Reparatur-Gene in Krebszellen fehlen, sind diese unfähig, sich nach der Bestrahlung selber zu reparieren. Dies konnten die Forschenden im Tiermodell und in menschlichen Zellen nachweisen. Wenn diese Gene fehlen, besteht somit eine gute Chance, dass die Strahlentherapie erfolgreich sein wird. «Unsere Erkenntnisse zeigen, wie wichtig eine personalisierte Krebstherapie ist, welche die genetische Prädisposition der Betroffenen berücksichtigt», sagt Rottenberg.
International vernetzte und von der EU unterstützte Forschung
Mit dem Ziel, die Forschung für solche personalisierten Therapien zu stärken, hat die Universität Bern 2019 das Zentrum für Präzisionsmedizin gegründet. Es soll dazu beitragen, massgeschneiderte Therapien für Krebspatientinnen und -patienten zu entwickeln. Zur Erforschung der Strahlentherapie arbeitet die Gruppe von Prof. Rottenberg neben dem niederländischen Krebsforschungszentrum auch mit Forschungsgruppen der Universität Zürich, der Oxford University und dem Dana-Farber Cancer Institute in Boston zusammen.
Die Forschung von Sven Rottenberg wird unterstützt vom Schweizer Nationalfonds (SNF), der Schweizer Krebsliga, der Novartis Stiftung für medizinisch-biologische Forschung und der Wilhelm Sander Stiftung. Ausserdem erhält er Unterstützung vom European Research Council (ERC), der exzellente Forschung im Rahmen von Horizon 2020 fördert.
Bern Center for Precision Medicine (BCPM)Das Bern Center for Precision Medicine (BCPM) wurde 2019 auf Initiative und mit Unterstützung des Kantons, der Universität Bern und Inselspital, Universitätsspital Bern, gegründet. Das BCPM ist in Forschung, Vernetzung und Ausbildung aktiv. |
Publikationsdetails:Francica P, Mutlu M, Blomen VA, Oliveira C, Nowicka Z, Trenner A, Gerhards NM, Bouwman P, Stickel E, Hekkelman ML, Lingg L, Klebic I, van de Ven M, de Korte-Grimmerink R, Howald D, Jonkers J, Sartori AA, Fendler W, Chapman JR, Brummelkamp T, Rottenberg S (2020). Functional radiogenetic profiling implicates ERCC6L2 in non-homologous end joining. Cell Reports, 25. August 2020, https://www.cell.com/cell-reports/fulltext/S2211-1247(20)31053-6 |
25.08.2020